![]() Set centres hospitalaris de la capital espanyola han participat en la fase II de l’assaig clínic Aplicov, impulsat per la farmacèutica PharmaMar, amb un fàrmac anticancerígen (Aplidin) que ha aconseguit reduir la càrrega viral en pacients adults amb Covid que han requerit ingrés hospitalari.
Set centres hospitalaris de la capital espanyola han participat en la fase II de l’assaig clínic Aplicov, impulsat per la farmacèutica PharmaMar, amb un fàrmac anticancerígen (Aplidin) que ha aconseguit reduir la càrrega viral en pacients adults amb Covid que han requerit ingrés hospitalari.
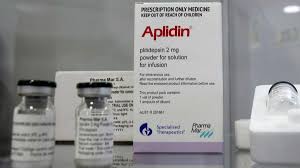 El conseller de Sanitat, Enrique Ruiz Escudero, ha assistit aquest dilluns a la presentació dels resultats preliminars de l’assaig realitzat en 13 hospitals espanyols, set d’ells madrilenys, amb la molècula Plitidepsina, que ha aconseguit els objectius de seguretat i d’eficàcia.
El conseller de Sanitat, Enrique Ruiz Escudero, ha assistit aquest dilluns a la presentació dels resultats preliminars de l’assaig realitzat en 13 hospitals espanyols, set d’ells madrilenys, amb la molècula Plitidepsina, que ha aconseguit els objectius de seguretat i d’eficàcia.
Els investigadors han detallat els aspectes més concrets d’aquest estudi els «resultats preliminars del qual són esperançadors en reduir de manera significativa la càrrega viral dels pacients, així com els nivells de Proteïna C-reactiva».
Aquesta proteïna, que es produeix al fetge com a resposta a la inflamació, és un marcador comú que apareix alterat en tots els pacients que pateixen covid-19 a causa de les característiques inflamatòries que implica el virus.
 L’estudi ha avaluat la seguretat i eficàcia en tres grups de pacients amb tres nivells de dosis diferents de plitidepsina, administrats per via intravenosa, durant tres dies consecutius en pacients amb coronavirus, que requereixen hospitalització.
L’estudi ha avaluat la seguretat i eficàcia en tres grups de pacients amb tres nivells de dosis diferents de plitidepsina, administrats per via intravenosa, durant tres dies consecutius en pacients amb coronavirus, que requereixen hospitalització.
L’administració de la plitidepsina s’ha mostrat eficaç en la reducció aguda de la càrrega viral. Una altra dada significativa és que entre el 80-90% dels pacients van ser donats d’alta mèdica abans del dia 14 d’hospitalització i un 38% abans del dia 8, presentant molts d’ells la negativización de la PCR en aquestes dates
El director clínic de Pharmamar, José Jimeno, ha dit que, després de comprovar els «resultats positius» del fàrmac Aplidin en pacients adults amb covid-19 que requereixen hospitalització, ara l’objectiu principal de l’empresa és sol·licitar a les agències reguladores el permís necessari per a posar en marxa un assaig en Fase III «el més aviat possible».
 Per a això, en les pròximes setmanes, Pharmamar discutirà «d’una manera lineal, honesta, ètica i directa» amb les agències reguladores, com l’Agència Espanyola del Medicament i la FDA estatunidenca, perquè s’aprovi un assaig amb més pacients que permeti comparar els resultats del fàrmac amb els tractaments actuals contra el coronavirus, principalment corticoides.
Per a això, en les pròximes setmanes, Pharmamar discutirà «d’una manera lineal, honesta, ètica i directa» amb les agències reguladores, com l’Agència Espanyola del Medicament i la FDA estatunidenca, perquè s’aprovi un assaig amb més pacients que permeti comparar els resultats del fàrmac amb els tractaments actuals contra el coronavirus, principalment corticoides.






